新冠病毒(SARS-CoV-2)感染可导致新冠肺炎(COVID-19),新冠病毒感染重症患者的症状可发展为急性呼吸窘迫综合征(ARDS),进一步导致多组织器官损伤、甚至死亡。已有研究表明,细胞因子风暴(Cytokine Storm)是新冠患者病情恶化的主要临床特征,也是决定新冠肺炎预后的关键因素。因此,阐述新冠病毒诱导细胞因子风暴的分子机制对于防治新冠肺炎至关重要。
低氧诱导因子1α(HIF-1α)在细胞增殖和血管生成等生理过程中起着重要的调节作用,同时也在调节代谢途径和炎症反应中起关键作用。HIF-1α能促进细胞糖酵解过程,诱导巨噬细胞炎症反应;而HIF-1α的失调可促进多种疾病的发生发展,包括:癌症、代谢性疾病、心脑血管疾病以及阿尔茨海默症等;充分表明HIF-1α在机体疾病进程中具有重要功能、起着关键作用。但是,新冠病毒诱导HIF-1α表达的作用机制以及HIF-1α在调控新冠病毒感染和细胞因子风暴产生中的功能及其作用机理仍不清楚。
2021年8月18日,暨南大学吴建国教授研究团队在Nature子刊《Signal Transduction and Targeted Therapy》杂志上在线发表了题目为“HIF-1α promotes SARS-CoV-2 infection and aggravates inflammatory responses to COVID-19”的文章。该研究成果揭示了HIF-1α在新冠病毒感染导致的细胞因子风暴中的关键作用及其作用机制。这一成果是该团队于2021年8月2日在Nature子刊《Nature Communications》发表题为“SARS-CoV-2 N protein promotes NLRP3 inflammasome activation to induce hyperinflammation”文章后,在新冠病毒感染与致病机制研究领域的又一重要成果。

研究团队通过对新冠病人的外周血单核细胞(PBMC)的转录组测序分析(RNA-Seq)以及新冠病毒感染实验发现,HIF-1α信号通路、免疫反应以及代谢途径等在病毒感染后显著失调。通过深入研究证明,新冠病毒的 ORF3a蛋白通过诱导线粒体损伤和线粒体活性氧(ROS)产生,促进HIF-1a表达。进一步研究发现,HIF-1a接下来能促进新冠病毒感染与复制、诱导细胞炎症因子过度表达、加速细胞损伤。相反,HIF-1α的特异性抑制剂可有效抑制新冠病毒感染与复制、降低细胞炎症因子的表达、减弱细胞损伤。
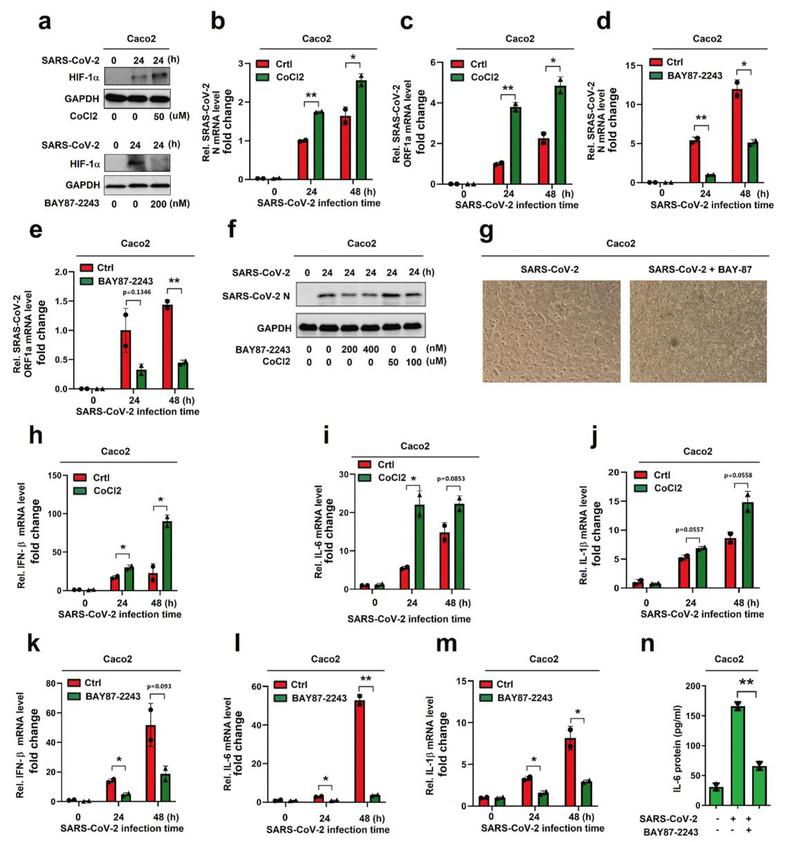
因此,该项研究揭示了新冠病毒感染诱导细胞因子风暴的新机制,证实HIF-1α在新冠病毒感染诱导过度炎症反应和导致细胞损伤中发挥了关键作用,提出靶向HIF-1α的抑制剂是防治新冠肺炎的潜在药物。
暨南大学吴建国教授为论文的通讯作者、张其威教授和罗震副教授为论文的共同通讯作者;暨南大学博士后田明富为第一作者、华中科技大学刘为勇博士和湖北省疾病预防控制中心李翔博士为共同第一作者。该项研究工作得到国家自然科学基金重点项目等基金的资助。
论文链接:https://www.nature.com/articles/s41392-021-00726-w
吴建国教授团队:https://iommb.jnu.edu.cn/main.htm